Outros exames que avaliam a fertilidade
Frente a um parceiro com história reprodutiva alterada ou espermograma com alteração, mesmo que as técnicas de reprodução assistida possam resolver o problema, é importante uma avaliação por um urologista, de preferência com formação em andrologia. Muitas enfermidades graves podem cursar com alterações do espermograma, como tumores testiculares e pituitários. Não ter essa avaliação pode impedir um diagnóstico precoce.
Este profissional realizará um exame clínico completo, analisando a distribuição dos pelos pelo corpo, o que já pode dar noções superficiais sobre as condições hormonais do paciente, o pênis e os testículos. Os testículos devem ser avaliados no tamanho, consistência, volume, palpação dos ductos deferentes, epidídimos e a presença da varicocele (varizes escrotais) ou outras alterações.
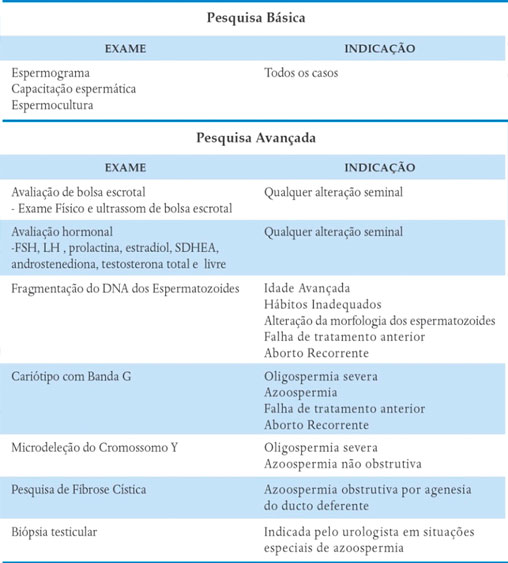
Quadro 1: Exames para pesquisa da fertilidade masculina
Ultrassom pélvico e de bolsa escrotal
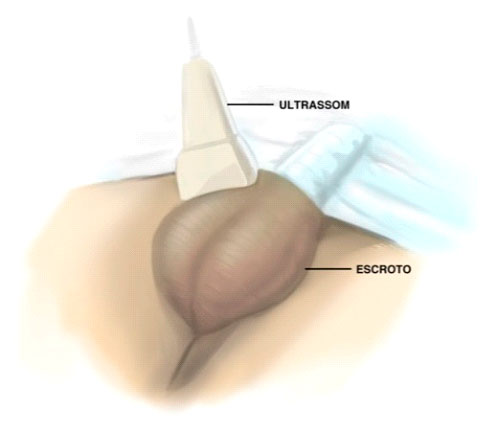
Por meio deste exame é possível avaliar a próstata, as vesículas seminais e, principalmente, o epidídimo e os testículos. Nesse último caso, avalia-se o tamanho e, com a ajuda do Doppler acoplado ao ultrassom, estuda-se o fluxo sanguíneo (varicocele), além de eventuais tumores.
Figura 1: Ultrassom de bolsa escrotal
Avaliação hormonal
Os principais hormônios avaliados são FSH, LH, testosterona total, testosterona livre, androstenediona, SDHEA e prolactina. Esses exames são indicados quando houver um espermograma com concentração muito baixa. Frente a esses resultados, poderá ser identificada se a origem da baixa quantidade é em decorrência de empecilhos para a produção, da própria produção ou na eliminação dos espermatozoides (causas pré-testicular, testicular ou pós-testicular).
Avaliação genética/cromossômica
Cariótipo com banda G: O cariótipo clássico com bandeamento é o primeiro exame para avaliar problemas cromossômicos e o mais simples que investiga alterações numéricas, translocações balanceadas e inversões – todas responsáveis pela infertilidade do homem e podendo causar problemas futuros no bebê que virá. A alteração mais comum de cariótipo é a síndrome de Klinefelter (47, XXY) que, em seu quadro clássico, cursa com quadro de hipogonadismo hipergonadotrópico e azoospermia, embora possa ter quadros clínicos variados e até ser possível haver produção de espermatozoides, raramente presentes no ejaculado. Acomete 11% dos pacientes azoospérmicos.
Outras alterações de cariótipo como inversões e translocações podem não causar repercussões no homem, mas estão relacionadas à infertilidade pelas formações de gametas com alterações cromossômicas.
Microdelação do cromossomo Y: O cromossomo Y é o que define o sexo masculino e é o menor do genoma humano. Tem três braços: dois curtos e um longo, que é dividido em três regiões chamadas AZFa, AZFb e AZFc, que contêm informações genéticas responsáveis pela produção e maturação dos espermatozoides. Chama-se microdelação a ausência total ou parcial das informações que estão no DNA dessas regiões. Microdelações são identificadas em 15% a 25% dos homens azoospérmicos e em 10% dos homens com produção dos espermatozoides gravemente comprometida, a chamada oligospermia severa (menos do que cinco milhões de espermatozoides por ml). Homens com quantidades maiores só em casos raros têm esse tipo de problema.
Essa alteração não é percebida no cariótipo normal, e só pode ser estudada por um exame específico no sangue pela técnica de PCR (Reação da Cadeia da Polimerase). Todos os homens portadores de microdelações devem receber aconselhamento genético e ser orientados sobre os tratamentos de infertilidade, a constituição de sua família, a herança genética aos filhos do sexo masculino e a possibilidade de tornar-se azoospérmico. A indicação preventiva do congelamento do esperma pode ser uma boa opção. Não existem outras implicações na saúde do indivíduo, e essa alteração só poderá ser herdada em bebês do sexo masculino. O tratamento da fertilidade é feito por técnicas de fertilização in vitro, geralmente buscando-se espermatozoides diretamente nos testículos.
Nos casos de azoospermia com presença de microdeleção na região AZFc, há boa chance de se encontrar espermatozoides no testículo. Se microdeleções nas outras regiões, as chances de se encontrar espermatozoides são muito pequenas.
Pesquisa de Fibrose Cística: A fibrose cística é uma doença autossômica recessiva que cursa com doença pulmonar progressiva, disfunção pancreática exócrina e concentração elevada de eletrólitos no suor. Os homens são inférteis por agenesia congênita ou hipoplasia de ductos deferentes, levando a um quadro de azoospermia obstrutiva. Em alguns quadros leves, esta é a única manifestação da doença. É possível gravidez com recuperação de espermatozoides diretamente no testículo, entretanto é importante o aconselhamento genético do casal, com pesquisa se a mulher é heterozigota, pelo risco de filho acometido. Nestes casos, pode ser realizado teste genético pré-implantacional.
outros: Existem outras alterações genéticas mais raras que podem ser pesquisadas na história familiar ou quadro clínico. Um exemplo é a Síndrome de Kartagener, doença autossômica recessiva que leva a uma discinesia ciliar, com deficiência no transporte muco-ciliar. Cursa com a tríade: sinusite crônica, bronquiectasia e situs inverso. Por alteração no flagelo do espermatozoide, podem apresentar infertilidade.
TAS: Teste de Aneuploidias no Sêmen – Análise de anomalias cromossômicas espermáticas: 5 cromossomos: 13, 18, 21, X e Y
O TAS ou em inglês SAT: Sperm Aneuploidy Test, é um teste para avaliar a fertilidade masculina e estuda a etiologia genética da infertilidade do homem. Permite analisar a presença de um número anormal de cromossomos (aneuploidias) nos espermatozoides e determina o risco de transmissão destas anormalidades e outras doenças cromossômicas aos futuros filhos, além de ser uma das causas de abortos.
Em casais com fator masculino grave, há um maior risco de transmissão de anomalias cromossômicas espermáticas a sua descendência. As únicas aneuploidias compatíveis com o nascimento são as trissomias (3 pares de um cromossomo) do 13 (síndrome de Patau), 18 (síndrome de Edwards), 21 (síndrome de Down) e dos aneuplodias dos cromossomos sexuais, incluindo monossomia do X (Síndrome de Turner) e Klinefelter. O TAS analisa no sêmen os cromossomos 13, 18, 21, X, e Y comumente envolvidos em abortos espontâneos e descendentes afetados com anormalidades cromossômicas, pela técnica hibridação fluorescente in situ (FISH – Fluorescent In Situ Hybridization). O teste TAS permite a identificação de homens com chances de sucesso reprodutivo baixo, ou seja, aqueles com menores taxas de gravidez, maior risco de aborto e de filhos com alterações cromossômicas. Assim, o teste TAS avalia fertilidade masculina e pode orientar o casal para um possível aconselhamento genético antes do inicio de um tratamento de reprodução assistida.
Um número aumentado de espermatozoides aneuploides no sêmen aumenta o risco de gerar embriões aneuploides.
